中國臺灣VHH合成文庫原理解讀
截至2023年7月,全球至少已有4款納米抗體藥物獲批上市。Ablynx公司研發的Caplacizumab(商品名為Cablivi?)納米抗體藥物,用于治療獲得性血栓性血小板減少性紫癜(aTTP)的成人患者,已于2018年8月31日獲歐洲藥物管理局(EMA)批準上市,后于2019年2月6日獲美國食品藥品監督管理局(FDA)批準上市。傳奇生物的CAR-T細胞產品——西達基奧侖賽(CARVYKTI,英文通用名CiltacabtageneAutoleucel)采用了獨特的二價納米抗體設計,是FDA批準的基于VHH的CAR-T產品,用于治療復發或難治性多發性骨髓瘤。Ablynx公司開發的另一款納米抗體藥物Ozoralizumab是人源化、三價的雙特異性納米抗體,由兩個抗人TNFα納米抗體和一個抗人血清白蛋白(HSA)納米抗體組成,已于2022年9月26日在日本獲批上市。康寧杰瑞研發的Envafolimab屬于PD-L1單域抗體Fc融合蛋白,已于2021年11月在中國上市。另外,目前有20多項納米抗體相關藥物進入到臨床階段。上海溪長生物技術的全人源 VHH 合成文庫,實用數據推動研究發展。中國臺灣VHH合成文庫原理解讀
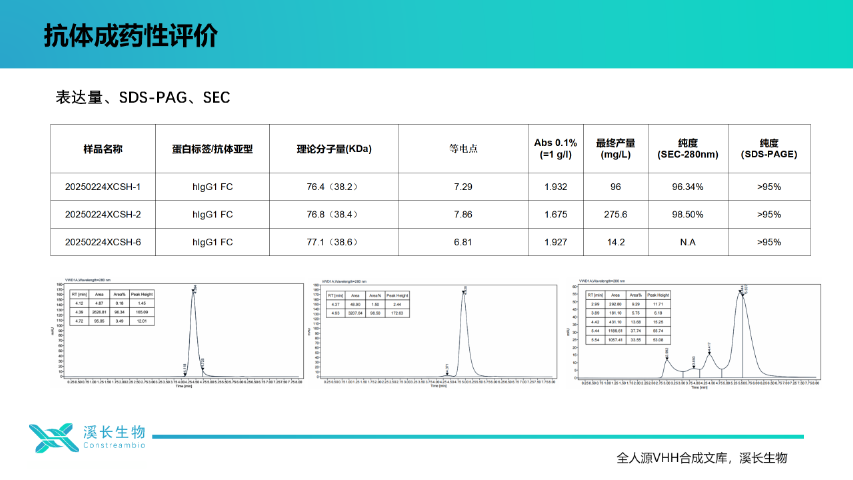
上海溪長生物全人源單結構域VHH合成文庫,致力于助力醫藥行業降本增效。通過提供快速、高效的抗體篩選解決方案,文庫能夠有效縮短藥物研發周期,降低研發成本。同時,文庫中的高親和力、高特異性抗體片段,能夠提高藥物的療效和安全性,為患者帶來更好的治療效果。文庫構建方法已申請多項發明專利,包括框架區設計、CDR突變策略及篩選流程優化。例如,通過改造FR2區四個關鍵氨基酸,明顯提升抗體的理化性質,同時保持與天然VHH相似的抗原結合模式。這種技術壁壘確保溪長生物在全人源VHH領域的競爭優勢。北京VHH合成文庫應用急需高效 VHH 抗體篩選?選擇上海溪長全人源單結構域(VHH)合成庫!
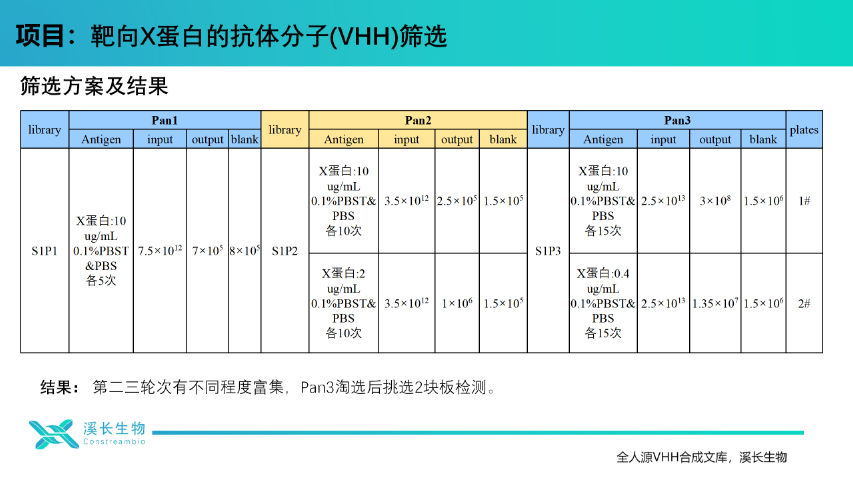
駱駝科動物的血清同時含有常規的異四聚體抗體和獨特的功能性重(H)鏈抗體(HCAb)。這些同二聚體抗體的H鏈由一個抗原結合結構域,納米抗體(VHH)和兩個恒定結構域(CH2,CH3區)組成。由于恒定結構域的缺失和納米抗體(VHH)側的重塑表面(通常與常規抗體中的L鏈相關),HCAb不能摻入輕(L)鏈。已經鑒定了構成HCAb的遺傳元件,但是仍在很大程度上對將這些抗體從其基因體內生成為抗原特異性和親和力成熟的真正抗體進行研究。然而,由多個晶體結構支持的抗原特異性VHH的簡便鑒定及其有益的生化和經濟特性(大小,親和力,特異性,穩定性,生產成本)鼓勵了將這些單域抗體用作研究工具以及生物技術和醫學的抗體工程化。
上海溪長生物全人源VHH合成文庫構建時針對CDR結合區,主要根據VH及VHH序列的CDR區長度統計,設計CDR中各區的長度及相對保守區域的氨基酸控制,通過Trimer技術可以控制每個位點氨基酸的比例,通常設計為等比例。CDR區長度通常針對CDR3的進行多種長度的平行設計,這是由于VHH的結合識別能力來自于其CDR3區loop環的長度,通過統計VHH的CDR3區長度較人源VH更長。極大地豐富了抗體的多樣性,能夠應對各種復雜抗原的挑戰,且截至目前已經成功交付了多個項目,交付質量好,客戶滿意度高上海溪長生物技術全人源 VHH 合成文庫,讓抗體研究更簡單高效。

VHH作為駱駝科動物特有的單鏈抗體,具有分子量小(約15kDa)、組織穿透性強、穩定性高的特點,在病毒中和、成像診斷等領域表現出獨特潛力。全人源VHH合成文庫將逐步替代部分傳統單克隆抗體,尤其在實體瘤、神經疾病等領域憑借穿透性優勢占據主導。同時,其與基因治療、細胞治療的融合應用(如作為AAV靶向配體)將加速遺傳病和罕見病治療的突破。此外,合成文庫結合高通量篩選的模式,可明顯降低中小企業的創新門檻,推動生物制藥創新生態的民主化,使抗體研發從“少數企業”走向“更廣的科研普惠”。全人源 VHH 合成文庫,上海溪長技術加持,抗體發現效率翻倍。北京VHH合成文庫應用
上海溪長生物技術全人源 VHH 合成文庫,更優的篩選流程提高開發效率。中國臺灣VHH合成文庫原理解讀
全人源VHH合成文庫在分子特性方面,完成了從小分子到大功能的突破;全人源VHH合成文庫產生的抗體分子量約15kDa,為單域結構,相比傳統IgG(~150kDa)或scFv(~25kDa),具有更強的組織穿透能力,在實體瘤中的穿透效率提升3倍,且能跨越血腦屏障,適合開發針對神經性系統疾病的藥物。其結構穩定性也明顯更優,可耐受極端pH環境(3-11)和蛋白酶降解,無需冷鏈運輸。此外,VHH可直接通過基因工程融合熒光標記或其他功能域,便捷構建雙特異性分子,而傳統抗體(如IgG)進行類似改造時需復雜操作,融合效率較低。中國臺灣VHH合成文庫原理解讀
- 新疆Fab合成文庫公司推薦 2025-12-20
- 廣西全人源單重鏈合成文庫流程解析 2025-12-20
- 山西單結構域文庫周期 2025-12-20
- 合成噬菌體文庫篩選方案 2025-12-20
- 陜西噬菌體文庫應用 2025-12-20
- 上海溪長生物VHH合成文庫篩選服務 2025-12-20
- 海南全人源單結構域(VHH)合成文庫項目合作 2025-12-20
- 青海Fab合成文庫篩選方案 2025-12-20
- 陜西合成文庫成本 2025-12-19
- 廣東全人源單重鏈合成文庫靶向開發 2025-12-19
- 植物生理研究植物表型平臺價格 2025-12-21
- 是什么聚醚醚酮生產企業 2025-12-21
- 常州醫用環氧乙烷滅菌價格 2025-12-21
- 哪里有六字真言香囊服務熱線 2025-12-21
- 常用哺光儀平臺 2025-12-21
- 吉林美容院拓客工具代理價格 2025-12-21
- 惠山區舒服健身器材批發 2025-12-21
- 欒川附近適合自理老人的醫護型養老院 2025-12-21
- 湖南一體化智能醫廢管理收集車生產廠家 2025-12-21
- 河南數字化醫院管理決策支持系統 2025-12-21