工業園區生物制品eCTD業務
美國eCTD驗證采用三級分類:“錯誤”(必須修正)、“警告”(建議修正)、“提示信息”(參考)。例如,PDF文件版本不符或加密保護屬于“錯誤”,而書簽路徑非相對性則可能列為“警告”。驗證失敗將直接導致退審,企業需通過LORENZ Validator等工具預檢,確保提交前合規。 技術驗證點 驗證涵蓋XML結構合規性、文件命名規則、生命周期管理(如序列號連續性)及PDF屬性(如字體嵌入、可搜索性)。臨床試驗數據需額外滿足CDISC標準,包括SDTM和ADaM數據集的結構驗證中IND注冊申報相關技術支持。工業園區生物制品eCTD業務

eCTD文件制作需遵循嚴格的法規要求和標準化流程,以下是關鍵要點整理:eCTD采用模塊化結構,包含模塊1(行政信息)至模塊5(臨床報告),需按ICH和監機構要求構建目錄樹。顆粒度選擇:文件提交層級需在***申報時確定并沿用,例如原料和制劑的章節(如、)需按比較低顆粒度拆分,輔料單獨成章。PDF需添加書簽(導航目錄)和超鏈接(跨網頁跳轉),超過5頁的文件必須包含目錄(TOC/LOT/LOF)。技術參數:初始視圖需設置默認縮放級別和頁面布局,書簽展開層級不超過三級,單文件大小需符合申報系統限制。驗證工具:使用軟件(如BXeCTD)自動生成書簽和超鏈接,并通過序列校驗和PDF校驗功能確保合規性。安徽ANDAeCTD軟件美國eCTD驗證標準相關技術支持。
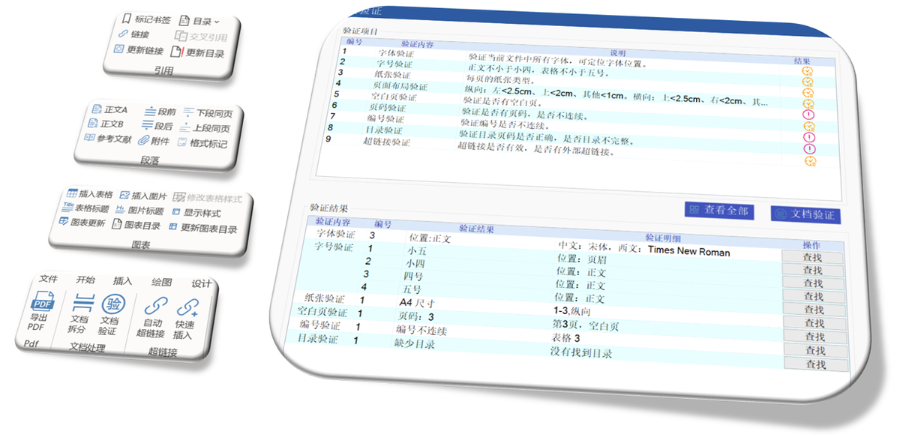
美國eCTD的強制實施時間與范圍:美國自2017年5月5日起要求申請(NDA)、仿制yao申請(ANDA)和生物制品許可申請(BLA)必須通過eCTD格式提交,2018年5月5日進一步擴展至臨床試驗申請(IND)和yao品主文件(DMF)。FDA通過《聯邦食品、yao品和化妝品法案》第745A條明確電子提交的強制性,豁免非商業化IND和部分DMF類型(如Ⅲ類)。2023年數據顯示,FDA接收的eCTD申請占比已達92%,標志著電子化審評體系的成熟。企業若未按規范提交(如缺少文件或重復序列號),將直接被拒收。
仿制yao作為提高yao物可及性與可負擔性的一類yao物,2012年以前,注冊審評是不收取任何費用的,但當時仿制yao申請積壓嚴重,從申報到獲批需要3~5年的時間。美國國會于2012年頒布了仿制yao使用者費用修正案(GenericDrugUserFeeAmendments,GDUFA),該法律要求制yao行業支付一定的用戶費用,以補充仿制yao申請的審評以及現場檢查的費用,減少仿制藥申請積壓,縮短審評時間,增加基于風險的現場檢查等,其目的是加快公眾獲得安全you效的仿制yao,并降低行業成本。GDUFA必須每五年重授權一次,于2017年更(GDUFAII),于2022年更(GDUFAIII);目前收費種類分為以下四種:ANDA審評費、DMF審評費,在審評時一次性繳納;項目費(Programfee)、設施費(Facilityfee),是上市后每年繳納一次。 加拿大IND注冊申報相關技術支持。

歐美eCTD實施經驗豐富,zhong國可借鑒以加速進程。zhong國可能會經歷從企業自愿eCTD提交到qiang制eCTD提交的過渡,且將緊隨ICH步伐,尤其在CMC資料整理方面。全球正向eCTD,zhong國也不例外,將隨日本、歐盟、美國等qiang制實施而逐步推進。zhong國崛起帶來全球化競爭機會,eCTD實施將助力zhong國企業走向世界。技術進步將加速eCTD實施,企業需密切關注技術動態,調整戰略。隨著國內就業壓力增大和企業出海需求增加,了解eCTD等guo際標準將成為職業發展的重要競爭力。zhong國推進eCTD需面對特色問題,如上市后申請資料匹配,需企業與監管機構共同解決。基線要求是關鍵,zhong國需制定適合國情的要求。期待未來執行指南既具特色又與guo際接軌,為eCTD實施提供支持。 eCTD注冊外包相關技術支持。杭州電子申報eCTD歡迎選購
瑞士eCTD注冊外包相關技術支持。工業園區生物制品eCTD業務
eCTD提交流程與ESG系統:FDA要求通過電子提交網關(ESG)傳輸eCTD文件,單個文件大小限制為10GB,超限需拆分或通過物理介質(如光盤)遞交。提交前需預分配申請號(如NDA編號),并通過ESG測試賬戶驗證技術合規性。序列號命名規則為4位數字(如0001),申請需從“原申請”序列開始,補充資料按遞增順序編號。企業可自愿提交預審樣本(Pre-Submission),FDA將反饋文檔結構、元數據等合規性問題。驗證標準與常見錯誤類型:FDA驗證標準分為高(High)、中(Medium)、低(Low)三級,高feng險錯誤(如無效XML或缺失關鍵表格)必須修復,否則直接拒收。常見問題包括:重復序列號(錯誤1034)、文件路徑超長(警告2015)、PDF加密或非標字體(錯誤4001)。2023年統計顯示,30%的提交因模塊1格式錯誤被退回,凸顯行政信息合規的重要性。驗證工具如LORENZeValidator被FDAguan方采用,可自動檢測200+項技術指標。 工業園區生物制品eCTD業務
- 楊浦區eCTD品牌 2025-12-20
- 河北仿制藥eCTD 2025-12-20
- 合肥NDAeCTD品牌 2025-12-20
- 吉林國際注冊eCTD 2025-12-20
- 無錫賦悅科技eCTD找哪家 2025-12-20
- 楊浦區國際注冊eCTD醫療科技 2025-12-20
- 徐匯區中國eCTD報價 2025-12-20
- 蘇州新藥eCTD 2025-12-20
- 北京加拿大eCTD 2025-12-20
- 靜安區CDE eCTD品牌 2025-12-20
- 浙江官方授權經銷Agilia再轉印打印機生產商 2025-12-23
- 準格爾旗現代數字化轉型影響 2025-12-23
- 甘肅吊裝工藝模擬數字孿生哪家好 2025-12-23
- 天津打印紙有幾種 2025-12-23
- 浙江PCBA的全自動功能測試一體化 2025-12-23
- 射洪進口工業組態網關 2025-12-23
- 吉林KC認證哪家性價比高 2025-12-23
- 北京推進**智能撰寫 2025-12-23
- 達拉特旗高速內存抖音代運營 2025-12-23
- 芯片堆疊封裝 2025-12-23