北京阿維巴坦
蘇尼替尼的臨床應用雖明顯改善了患者生存,但其毒性譜仍需嚴格管理。常見不良反應包括疲勞(發生率約60%)、腹瀉(50%)、手足綜合征(40%)及血壓高(35%),這些癥狀多與藥物對正常組織的非特異性抑制相關。骨髓抑制方面,3-4級中性粒細胞減少和血小板減少的發生率分別為12%和8%,需定期監測血常規。罕見但嚴重的不良反應包括左心室射血分數下降(發生率約3%)、肝毒性(ALT/AST升高至ULN5倍以上者占2-3%)及甲狀腺功能減退(15%)。針對心臟毒性,研究顯示基線射血分數<50%或醫治中下降≥20%的患者需停藥或減量;對于肝損傷,若膽紅素升高至ULN3倍以上,應暫停用藥直至指標恢復。此外,蘇尼替尼可誘導皮膚黃染(因代謝產物沉積)及黏膜炎,需通過保濕霜、止痛藥等支持醫治緩解。育齡期女性醫治期間需嚴格避孕,哺乳期婦女應停止哺乳,因其乳汁中藥物濃度可達血漿的12倍,可能對嬰兒造成嚴重不良反應。原料藥的質量控制包括純度、穩定性和微生物限度等指標。北京阿維巴坦
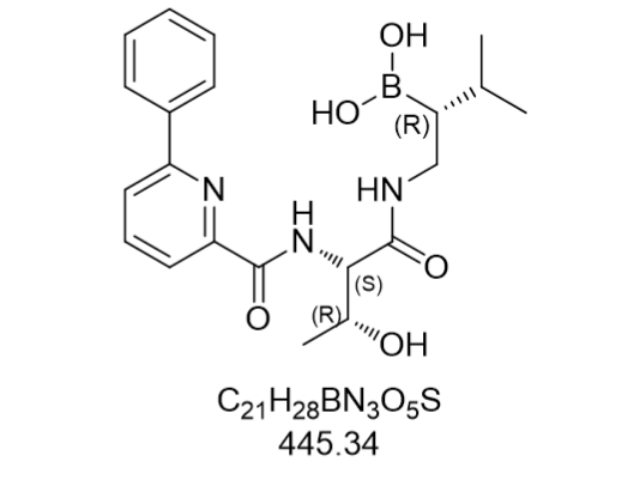
在臨床應用層面,艾沙佐咪與來那度胺、的聯合方案已成為復發/難治性多發性骨髓瘤的標準醫治選擇。TOURMALINE-MM1全球Ⅲ期臨床試驗納入722例患者,結果顯示聯合方案組的中位無進展生存期(PFS)達20.6個月,較對照組的14.7個月明顯延長。中國亞組分析進一步證實,亞洲患者群體中聯合方案組的總緩解率(ORR)達62%,其中完全緩解率(CR)為19%。值得注意的是,該方案采用全口服給藥模式,患者只需每周服用1次艾沙佐咪(4 mg),配合每日來那度胺(25 mg)和每周(40 mg),極大提升了醫治依從性。2017年《中國多發性骨髓瘤診治指南》將其列為二線醫治選擇的方案,2023年更新的NCCN指南更將其納入維持醫治推薦。北京阿維巴坦酶催化技術使原料藥合成步驟從8步縮減至3步,原子利用率提升35%。
在醫藥領域,5-氨基乙酰丙酸鹽酸鹽憑借其獨特的光動力特性成為第二代光敏劑的重要成分。當其被導入疾病組織后,可在特定波長光照射下轉化為原卟啉IX(PpIX),后者通過光化學反應產生單線態氧和自由基,選擇性破壞疾病細胞并啟動免疫應答。這種非侵入性醫治方式已普遍應用于皮膚疾病、腦膠質瘤等體表及淺層疾病的診療,其復發率低、痛苦小的優勢明顯優于傳統療法。此外,該物質在皮膚科領域展現出多重療效:針對HPV被染引發的尖銳濕疣、尋常疣,其光動力療法可實現90%以上;對炎癥性皮膚病,通過調節皮脂腺分泌和角質形成細胞增殖,可明顯改善癥狀。2017年美國FDA批準其作為神經膠質瘤術中可視化輔助手段,進一步拓展了其在精確醫療中的應用邊界。
地拉羅司(Deferasirox),化學編號為CAS:201530-41-8,是一種重要的藥物成分,它在醫治鐵過載癥方面展現出了良好的功能。地拉羅司作為由美國FDA批準的常規使用口服驅鐵劑,自2005年獲批以來,已在80多個國家上市,并被普遍應用于臨床。它的主要功能是幫助人體排除多余的鐵負荷,這對于那些因長期輸血醫治而導致體內鐵積累過多的患者尤為重要。例如,對于2歲及以上因輸血造成的慢性鐵負荷過多的患者,以及10歲以上非輸血依賴性地中海貧血(NTDT)綜合征患者,地拉羅司都能有效減輕他們的鐵過載情況,預防并發癥的風險。它還能明顯降低心臟、肝臟的鐵負荷,提高患者的生活質量。地拉羅司的用藥劑量通常根據患者的體重和鐵過載程度進行個體化調整,以確保達到很好的療效。長期使用高劑量的地拉羅司可能會面臨肝功能異常的風險,因此在使用期間需要定期進行肝功能監測。原料藥的市場競爭激烈,企業需不斷創新以保持優勢。
硼替佐米(CAS號179324-69-7)作為蛋白酶體抑制劑的標志藥物,不僅在科學研究領域引起了普遍關注,也在臨床實踐中展現了其獨特的價值。該藥物的開發與應用,標志著疾病醫治策略的一個重要轉變,即從傳統的非特異性細胞毒作用向更加精確地針對疾病細胞特定生存機制的方向發展。硼替佐米通過精確作用于疾病細胞內的蛋白酶體系統,實現了對疾病細胞生長和生存的精確打擊,同時盡量減少對健康細胞的傷害。這種高度選擇性的醫治方式,不僅提高了醫治效果,還明顯降低了患者的醫治負擔和不良反應。隨著對硼替佐米作用機制的深入研究和臨床經驗的積累,科學家們正探索其與其他療法聯合使用的潛力,以期進一步拓寬其應用范圍,為更多疾病患者帶來福音。原料藥的生產過程優化需結合生產效率,提高產量。北京阿維巴坦
原料藥的生產工藝優化可降低成本,提高生產效率。北京阿維巴坦
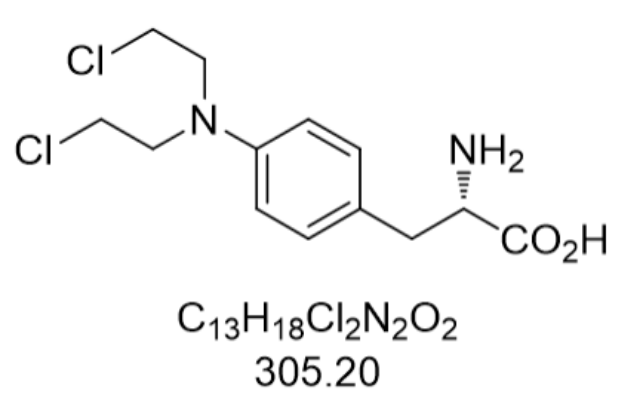
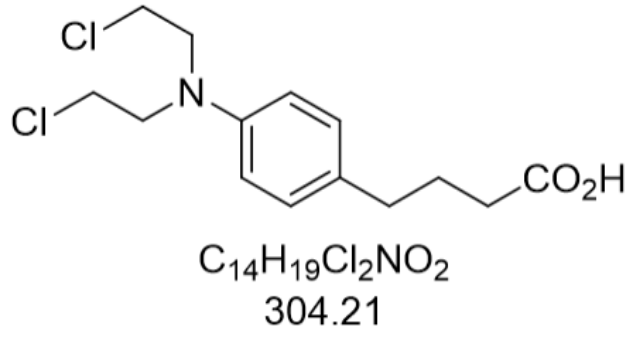
安全性評估數據顯示,美法侖的毒性特征呈現劑量依賴性與醫治窗狹窄特點。急性毒性研究中,大鼠腹腔LD50為4.484 mg/kg,小鼠皮下LD50為32 mg/kg,提示臨床需嚴格監控血藥濃度。主要不良反應包括骨髓抑制(Ⅲ-Ⅳ度中性粒細胞減少發生率65%)、胃腸道反應(惡心嘔吐發生率40%)和繼發惡性疾病(醫治5年后第二原發疾病風險增加3倍)。特殊人群用藥的方面,老年患者(>65歲)的3-4級不良反應發生率較年輕患者高20%,需進行劑量調整。生殖毒性研究顯示,妊娠期用藥可導致胎兒肢體短缺畸形(發生率約15%),哺乳期婦女用藥后乳汁中藥物濃度可達血藥濃度的30%,因此禁用于妊娠及哺乳期女性。長期隨訪發現,接受累計劑量>200 mg/m2的患者,5年后發生急性髓系白血病的風險為2.3%,這一數據支持臨床采用分次給藥的方案以降低遠期毒性。北京阿維巴坦
- 五氟本肼規格 2025-12-23
- 5-氨基乙酰丙酸鹽酸鹽采購 2025-12-23
- (4-溴苯)乙胺售價 2025-12-23
- 陜西硼替佐米-N-1Bortezomib-N-1硼替佐米中間體 2025-12-22
- 長春N-(2-(二乙基氨基)乙基)-2 2025-12-22
- N-BOC-L-脯氨醇哪里買 2025-12-22
- 2-環己酮甲酸乙酯廠商 2025-12-22
- 浙江(3-(溴甲基)-1-甲苯磺酰氮雜啶-3-基)甲醇 2025-12-22
- 反式-(1R 2025-12-22
- 銀川1-(3-吡啶基)-3-(二甲氨基)-2-丙烯-1-酮 2025-12-21
- 河南傳輸穩定智能垃圾分類回收秤價格 2025-12-23
- akg保健品新西蘭 2025-12-23
- 長寧區什么是醫療管理服務加盟 2025-12-23
- 杭州裝個智能假肢價格 2025-12-23
- 江西均相化學發光均相發光應用領域 2025-12-23
- 新疆是什么助膝器功效 2025-12-23
- 廣州質量好的nmn制造廠家 2025-12-23
- 廣東混合痔痔瘡套扎器生產廠家 2025-12-23
- 上海3M環氧乙烷滅菌檢測服務 2025-12-23
- 湖北美容院拓客工具生產企業 2025-12-23